马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
本帖最后由 Emj 于 2020-1-4 09:56 编辑
0 A/ b7 D, x* ^8 N+ P
: Y' B0 k0 P, N: y9 Y! w. I 随着医学的不断发展,实体瘤疗效评估也随之变迁,从1981年首次发表的WHO,2000年RECIST,2009年免疫时代相关疗效irRC,直到伴随着免疫检查点抑制剂的飞速发展,2017年更符合临床实践的评估标准:iRECIST诞生,使得更多患者在逐渐完善的评估标准下获得OS收益。5 ]- R- o: ?# G3 F9 J' g9 `$ N
接下来,Vv带你敲重点,轻松实用的掌握免疫治疗过程中的iRECIST。, P7 w( Z3 M6 c6 u0 u# x
1. RECIST) I7 {+ V8 i, w* g6 u7 F
RECIST是由临床研究者、制药行业、影像学专家、美国国立癌症研究所(NCI)、加拿大国立癌症研究所(NCIC)、英国癌症研究网络(NCRN)、欧洲癌症研究和治疗组织(EORTC)共同制定,主要针对实体瘤的疗效评价的标准。(非实体瘤不适用,如血液)/ F2 x2 N! g) o }* f
2.实体瘤测量方法:单径测量法
, }/ j) J) m' E5 ? 至少有一条可以准确测量的直径(记录为最大径)。, S& b# L2 E' |/ k' E! I
 * W2 ~" D" N* H, N8 K
* W2 ~" D" N* H, N8 K
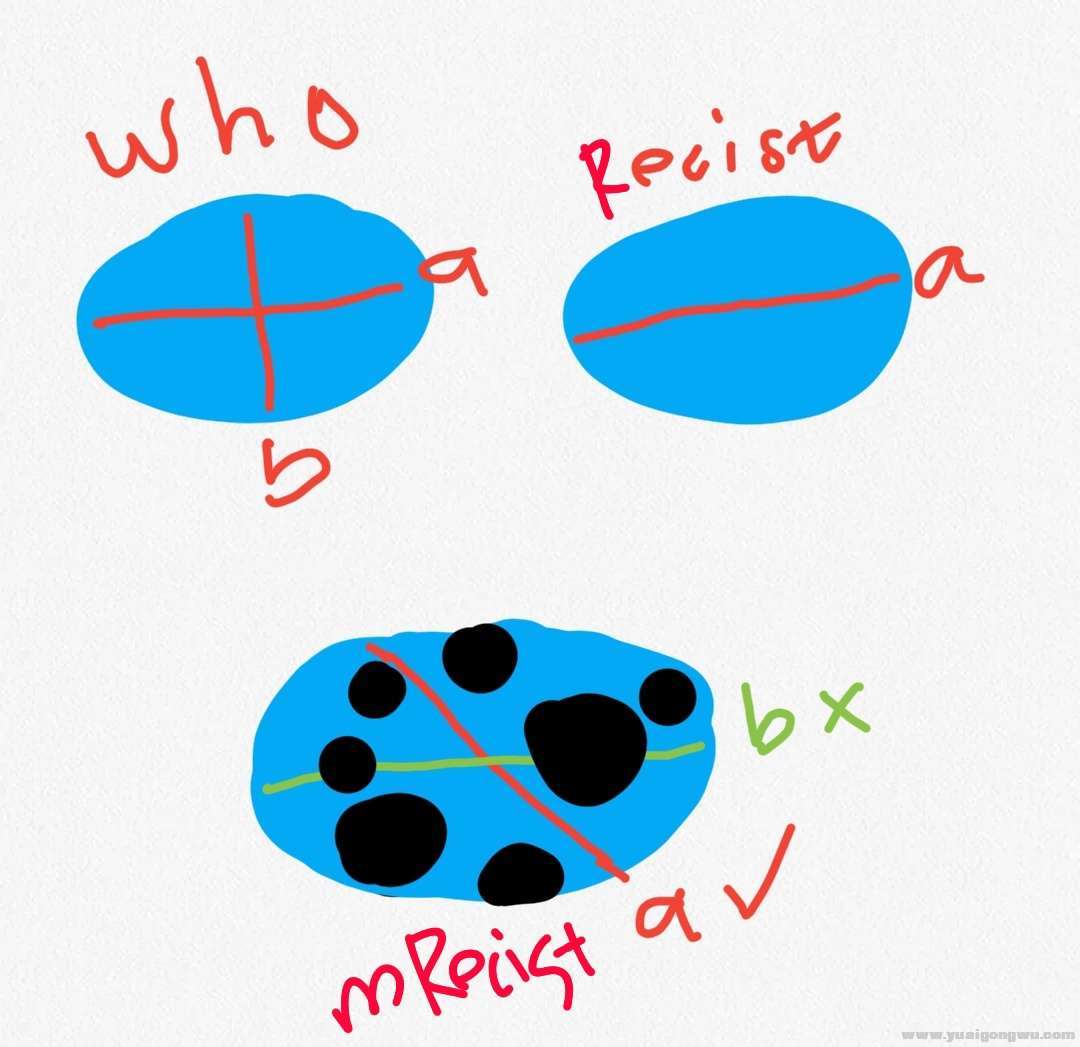
肿瘤的直径(RECIST)变化可较双径乘积(WHO)的变化更好的反映肿瘤细胞的变化,重复效果好,减少误差。mRECIST以“存活肿瘤”作为评估对象(排除坏死肿瘤的干扰)。2 P; C+ E- a6 W
注:免疫治疗过程中,治疗有效,病灶常呈现变薄,变淡,中央镂空,内部瓦解至不可测量的影像特征。
$ k1 y6 S1 e/ Z7 @" I3.可测量病灶
. K7 B2 q/ W5 q 它至少在测量平面上的一个直径线上能够被准确测量并记录。6 n% ~3 F% w& R9 m* @
可测量非淋巴结肿瘤病灶:测量最长直径。
) A7 V# h4 Q- T可测量恶性淋巴结: 测量最短直径。$ K5 W! J$ o V9 R% c5 m
4.不可测量病灶9 v' s8 {4 |5 k' X5 B2 |# o
病理性淋巴结:最短直径≥10mm且<15mm。
0 R1 d9 }* J9 x, s 非淋巴结:CT扫描最长直径<10mm。! C& j( |2 k; x2 h# R2 e0 H0 l
注:轻骨髓炎、脑膜病变、腹腔积液、胸腔积液、心包积液、炎性乳腺病、皮肤或肺的癌性淋巴管炎、腹部肿块/腹腔器官肿大等,影像学不能被测量需通过物理检查确定的病灶也是不可测量病灶。4 v7 M3 C& N0 q
5. iRECIST" @1 z' I. H& h
iRECIST(modified RECIST1.1 for immune based therapeutics, iRECIST4 }8 Y3 p; D1 x& k5 x! |; Z
iRECIST引入了iUPD概念(待证实的疾病进展),动态评估免疫治疗过程中可能出现的非典型模式。因此,只要患者临床稳定情况下,处方医生在判断iUPD后仍继续现有的治疗。
- ~5 F @7 ^6 i5 Z; o" M待证实的疾病进展(PD需要被证实)
# v. c) B: G7 S# W4 W$ o/ [待证实:
O* A$ Y7 H; P1 y, j1 ^7 G5 ^8 ~病灶进展或出现新病灶符合iRECIST)→IUPD4 [& w3 c& z( I1 \/ S( u6 y% w
IUPD符合iRECIST→iSD/iPR/iCR
6 | w! U' W5 _0 x% _7 O/ y G* c确认:( J) D$ m/ L5 g* ~3 M
原IUPD进一步恶化→PD
/ z" F( Y4 e& I2 | 未IUPD病灶符合RECIST1.1进展→PD
; A% L1 Z( j) P4 e! i
% S) F K, B# L6 j1 A% I/ U( F. M, v, E) h
/ `: F+ {( V3 d4 s9 x* s7 w
 . q, S+ q+ Q8 @( Z2 m
. q, S+ q+ Q8 @( Z2 m
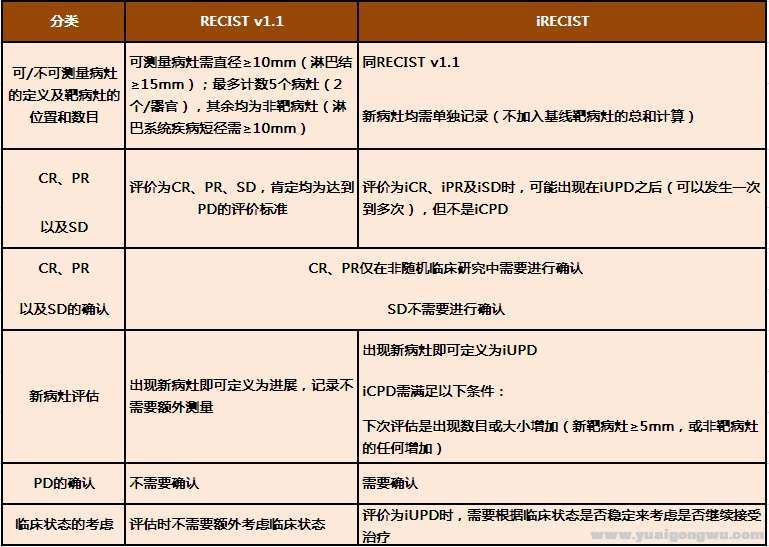
注:临床状态稳定的评估方式:' t) V& B8 K, z+ ?/ D% ^
1、患者体力活动状态(PS)评分没有下降
_0 [+ D, W$ ~: ]6 T2、疾病相关症状没有加重:如疼痛、呼吸困难 y ]$ ^0 H$ e" @# f8 h
3、无需增加疾病相关症状的治疗措施。- E. U2 b n& i+ Z/ R- R1 d! Y, ^
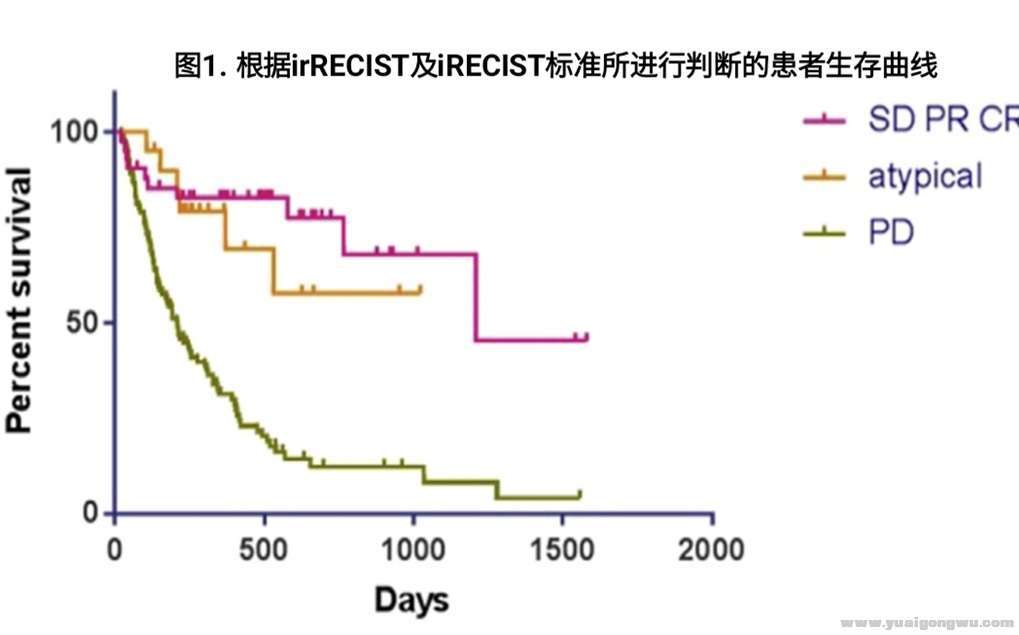
6.非典型缓解模式
6 W& t7 J2 w0 f* h T: J2 @主要表现为:延迟应答 假性进展 分离反应
# m- ~0 r# Z5 E- H: |) K一项PD1/ PDL1抑制剂治疗转移性NSCLC的临床研究(n=160)显示,在接受免疫治疗的患者中13%的患者发生非典型缓解模式,其中8例为假性进展,RECIST1.1低估了11%实际治疗有效的患者。
! K* v' U* o3 x) r/ ?- ]4 O* Q" g0 t# L+ A6 \2 q. D
' R( y0 C& t8 J- n

1 V u% h0 u1 E F. F: N/ ]8 w
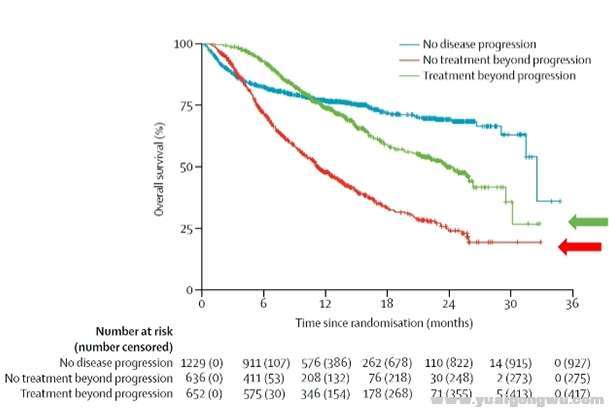
6 i8 }' o2 A2 d7.疾病进展后继续治疗TBP(有争议)
! A; V0 k7 ^; O' ~. t, H: g按照RECIST评估,IO治疗无效或耐药后,患者未出现疾病快速进展,对免疫治疗有良好的耐受性,继续使用,仍有19%的患者可能有效,可延长一倍的生存期24.4个月vs11.2个月(彻底放弃免疫治疗)
7 H$ ^: I8 v& n4 L' v8 M+ S/ k' ~
; l7 U4 j3 e$ W! i# ]- D8.超进展+ D; |4 d# ?0 Q. J# V" b
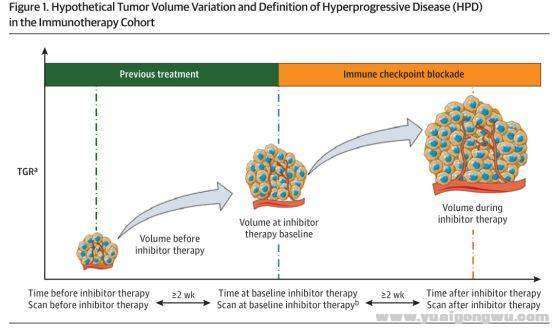
接受免疫治疗后,肿瘤反常加速生长,病情急剧恶化,这种现象称为超进展(Hyperprogression Disease,HPD)。. o2 R/ o8 W i0 y) W8 z) v
HPD应有严格的时间窗口和评估界定:
+ z% Z& A! A( C% q3 S- ](1)在免疫检查点抑制剂治疗后第一次评价时进展,至治疗失败时间(TTF)﹤2月;
) s5 P N( L9 [/ F% {: N' W(2)肿瘤体积增加>50%;/ i4 e; E6 N. ?5 I2 ^" e% L
(3)肿瘤增长速度(TGR)增加>2倍。/ @- l2 L; k; |5 X: [9 j2 B
若出现HPD症状,建议尽早考虑由免疫疗法转向抢救化疗。
8 y$ M) T/ t) E& b
' o1 [' l, ]& \: u/ F0 j" y. l+ K9. MDM2/ MDM4扩增与超进展相关性' P0 G( A2 j. T$ f# w
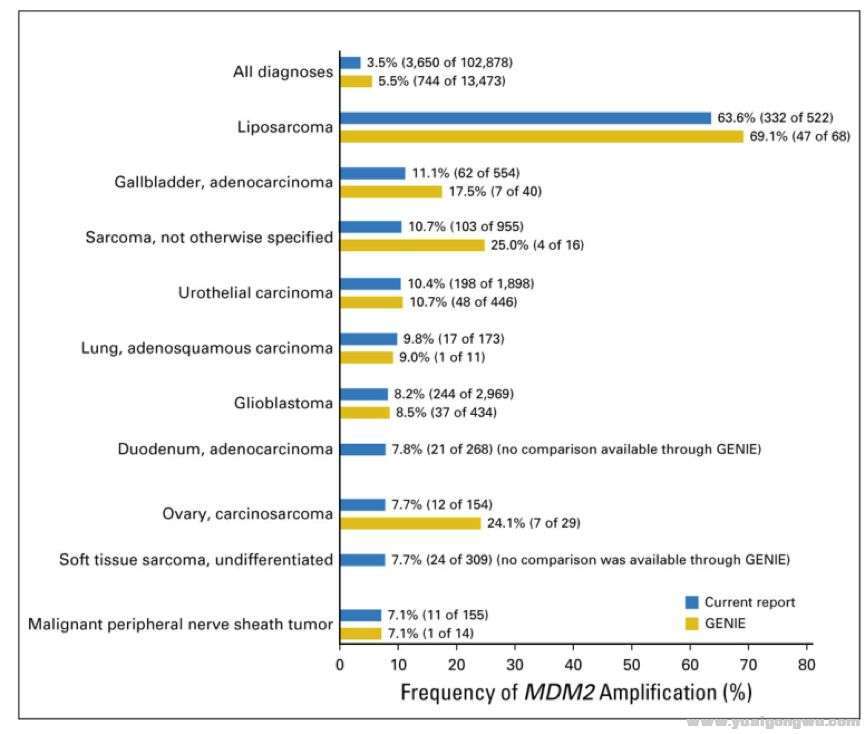
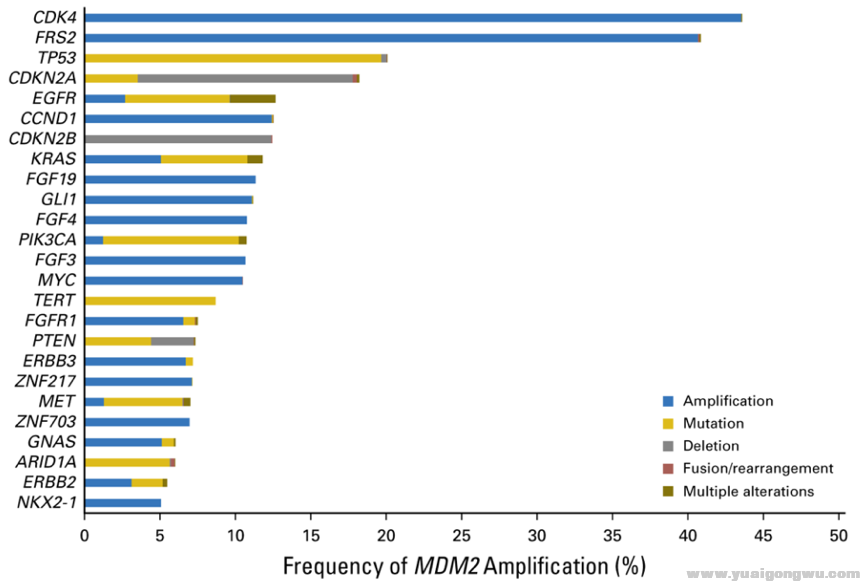
2017年3月,Kato等在CCR上报道了在155位肿瘤患者中,经免疫药物治疗后,TTF(time to treatment failure)<2个月的6位患者(均为接受PD-1/PD-L1抑制剂治疗的患者),都具有MDM2/MDM4扩增。
% O; }' S) { | c) ` 2019美国临床肿瘤学会(ASCO)年会的摘要中,一项非小细胞肺癌(NSCLC)回顾性研究分析了20例一线帕博利珠单抗治疗的晚期患者,其中5例患者出现了HPD,研究者通过荧光原位杂交技术(FISH) 、免疫组化(IHC)和NGS分析(FoundationOne CDx,FMI)显示,5例HPD患者均存在MDM2扩增。& _: f9 ~9 ?4 I! J3 J$ W" X
注:CDKN2A/B基因缺失及MDM2改变与免疫HPD密切相关。
. R9 w9 ^/ F( s8 }
, D8 z0 w3 ]; a; a1 e
 - F2 D4 Z; P/ f: F$ `: B( @6 W1 X3 K
- F2 D4 Z; P/ f: F$ `: B( @6 W1 X3 K
免疫治疗仍处于探索,整理,反思的阶段,很多论证和观点也待随之改革,进化,逐步完善。
t9 z: }6 q& u" S5 w希望Vv与大家在学习探索的道路上,并肩作战。
8 l J( d% ~( j8 s9 Z3 V) f
 6 A2 U( d8 a3 t7 `1 X) y
6 A2 U( d8 a3 t7 `1 X) y
|
|
|
|
|
|
|
共31条精彩回复,最后回复于 2024-8-1 07:24

累计签到:1 天
连续签到:1 天
[LV.1]初来乍到
|
Vv的这篇科普文章不错,对于如何从影像角度正确分辨假性进展和超进展很有学习意义。而这两个也正是免疫治疗中非常关键,却又完全相反的两个结论。 |
|
|
|
|
|
|

尚未签到

尚未签到

尚未签到
|
CDKN2A/B基因缺失和错义突变是不一样吧?所以错义突变和HPD不是密切相关? |
|
|
|
|
|
|

尚未签到

尚未签到
不知道能教一下,这个问题一定关系到很多人。今天看到这样一个观点:基因扩增或者基因缺失驱动的癌症不适合使用PD1抗体免疫治疗。因为记得snoopy说过他父亲从临床相信上看有cmet扩增。能不能就这个观点做些相关数据收集和说说想法?! o8 `) y' A! j/ e/ I4 k( f
4 P" q& r$ d/ l. v
|
|
|
|
|
|
|

累计签到:3 天
连续签到:1 天
[LV.2]与爱新人
本帖最后由 Emj 于 2020-1-7 13:33 编辑 6 S+ K/ ~3 I0 a" W
香脸 发表于 2020-01-07 12:43
- l3 l7 x3 j, R* d Z不知道能教一下,这个问题一定关系到很多人。今天看到这样一个观点:基因扩增或者基因缺失驱动的癌症不适合使用PD1抗体免疫治疗。因为记得snoopy说过他父亲从临床相信上看有cmet扩增。能不能就这个观点做些相关数据收集和说说想法?
" K, |" j: i g% v& Y8 R( I7 V" S
“基因扩增和缺失不适合免疫”这句话范围很大,目前为止,没有任何足够证据证明哪些基因会导致超级展,往往是一些基因扩增和缺失会与一些超进展相关基因伴随出现,比如MDM2扩增。目前实验中的MDM2/4扩增和它的伴随基因,是在实验列队里唯一100%超进展的列队,所以认为,存在很强的相关性。 |
|
|
|
|
|
|

尚未签到
Emj 发表于 2020-01-07 13:32
0 z2 J& W7 K6 ~$ I8 t本帖最后由 Emj 于 2020-1-7 13:33 编辑
' [; H3 B& ~+ z# U& h; [" @/ |8 D6 Q" A! ^/ b% L$ c( H/ ]
5 x- v3 f- I1 n. e6 e
+ e) |( X( u; T4 U" K- K
“基因扩增和缺失不适合免疫”这句话范围很大,目前为止,没有任何足够证据证明哪些基因会导致超级展,往往是一些基因扩增和缺失会与一些超进展相关基因伴随出现,比如MDM2扩增。目前实验中的MDM2/4扩增和它的伴随基因,是在实验列队里唯一100%超进展的列队,所以认为,存在很强的相关性。
这个观点里说的不适合是指PD1 抗体不能识别基因扩增或基因缺失癌细胞 |
|
|
|
|
|
|

尚未签到
基因扩增或者基因缺失驱动的癌症不适合使用PD1抗体免疫治疗。相当于原发耐药。
; X! | e% P3 a$ T; J0 G& N. P* ]2 Z# X/ K3 G6 i
|
|
|
|
|
|
|

尚未签到